Date: March 2018
Wie wir im Modell-Spotlight des letzten Monats gezeigt haben, ist Lungenkrebs eine verheerende Krankheit und die häufigste Todesursache bei Krebs in den USA und weltweit.1 Die Forschungsgemeinschaft sucht weiterhin nach neuen Modellen, die in der Lungenkrebsforschung helfen werden. Das ATCC (ein weit genutztes Zell-Repository) verfügt derzeit über 100 verschiedene Lungenkrebszelllinien vom Menschen.
Da Lungenkrebs so weit verbreitet ist, gibt es zahlreiche Möglichkeiten, neue menschliche Linien zu erwerben und zu charakterisieren. Wissenschaftler sind mittlerweile hochqualifiziert darin, die Mutationen, die eine erhöhte Proliferation bewirken, von denen zu unterscheiden, die das Tumorwachstum unterdrücken. Diese Informationen sind der Schlüssel zur Entwicklung neuartiger Therapien zur Behandlung von Lungenkrebs.
Labcorp continues to investigate new and/or unconventional cell lines and understand their importance to our client's research. In diesem Modell-Spotlight werden wir einige dieser Linien vorstellen und erläutern, wie wir unser Fachwissen als wertvolle Ressource für unsere Kunden nutzen, die künftige Behandlungen entwickeln möchten.
NCI-H3122
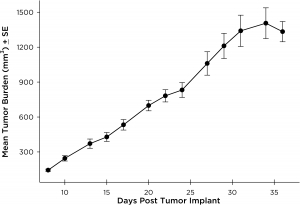
NCI-H3122 wurde 1981 von einem primären bronchioalveolären Lungenkarzinom eines 52-jährigen Mannes vor der Behandlung gewonnen. Diese Zelllinie enthält das EML4-ALK-Fusionsprotein (Echinoderm-Mikrotubuli-assoziiertes Protein-ähnliches 4 fusioniert mit dem anaplastischen Lymphomkinase-Gen) und wurde kürzlich in ca. 7 % der japanischen NSCLC-Patienten (nicht-kleinzelliger Lungenkrebs) und ca. 4,5 % aller NSCLC-Fälle identifiziert. Das ALK-Gen ist aufgrund seiner Fähigkeit, onkogen zu sein, ein Ziel von Interesse. Da NCI-H3122 EML4-ALK enthält und hochempfindlich gegenüber ALK-Hemmstoffen mit einem einzigen Wirkstoff ist, scheint sein Überleben durch einen mehr von ALK abhängigen Pfad gesteuert zu werden.2 Als präklinisches Modell wäre diese Zelllinie zum Screening neuer ALK-Hemmstoffe geeignet, die nicht von EGFR oder anderen an NSCLC beteiligten Pfaden abhängig sind. The model has been developed as a subcutaneous (SC) implant; however, we have also implanted this line intracranially to mimic the clinical setting where advanced NSCLC metastasizes to the brain. Das subkutane Tumorwachstum ist zuverlässig und zeigt nur eine minimale Variabilität von Tier zu Tier. Die Verdopplungszeit des Tumorvolumens bei der subkutanen Implantation beträgt ca. 7 Tage und Mäuse erreichen typischerweise eine Bewertungsgröße von ca. 750 mm3 in ungefähr 25 Tagen. Erste Daten zu intrakraniell implantiertem NCI-H3122 sind ermutigend. In einer Pilotstudie haben wir eine Annahmerate von 100 % und eine Verdopplungszeit des Tumorvolumens (auf Grundlage der volumetrischen Bewertung) von ca. 7 Tagen gesehen, was mit der subkutanen Wachstumsrate übereinstimmt (siehe Abbildungen 1 und 2). Wie bei vielen intrakraniellen Modellen wird die Morbidität (Körpergewichtsverlust und klinische Gesamtbeobachtung) verwendet, um das Gesamtüberleben zu definieren. Für diese Zelllinie beträgt der mittlere Zeitpunkt bis zum Tod ca. 35 Tage (siehe Abbildungen 2, 3 und 4).
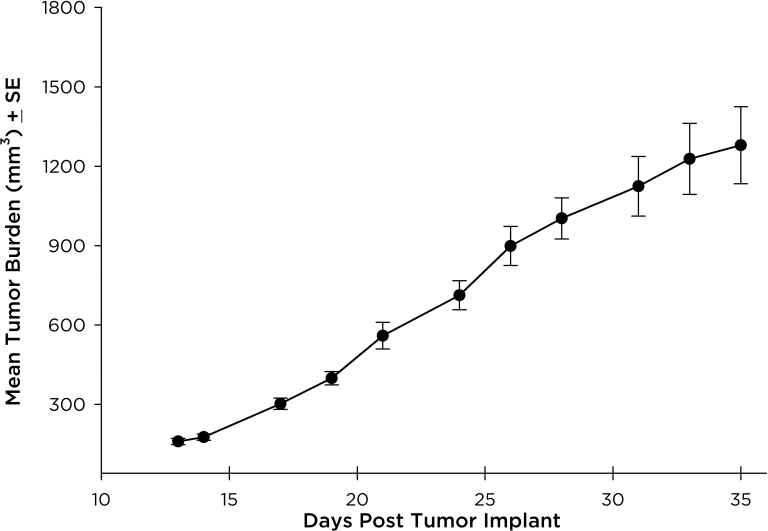
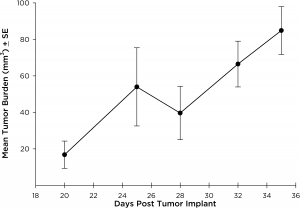
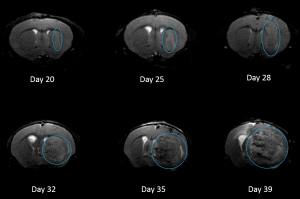
Abb. 1: Subkutanes NCI-H3122 – mittlere Tumorlast
Abb. 2: Mittleres intrakranielles NCI-H3122-Tumorwachstum mittels MRT
Abb. 3: Änderung des Körpergewichts in % nach intrakranieller Implantation von NCI-H3122
Fig. 4: H3122-3160 Representative Image
NCI-H1703
NCI-H1703 wurde aus einem Plattenepithelkarzinomen der Lunge eines 54-jährigen kaukasischen männlichen Rauchers im Stadium 1 gewonnen. Diese Zelllinie ist für die Forschungsgemeinschaft aufgrund der hohen Amplifikation des von Blutplättchen abgeleiteten Wachstumsfaktorrezeptors α (PDGFRα) von Interesse. NCI-H1703 is one of very few NSCLC models that have this expression profile and are sensitive to sunitinib in vitro. Klinisch sind Lungenkrebspatienten, die PDGFRα exprimieren, mit einer aggressiveren Tumorbiologie und einer schlechteren Prognose verbunden.3 Daher eignet sich dieses Modell zur Bewertung neuer angiogener Ziele wie VEGF sowie neuer PDGFRα-Ziele unabhängig von den Zelloberflächenproliferationswegen. The model is most commonly utilized following subcutaneous (SC) implant, however, we have also transfected this line with luciferase to allow for bioluminescence imaging to monitor disease progression following direct implant into the lung. Tumor growth is reliable following either SC or orthotopic (OT) lung implant. An beiden Implantationsstellen besteht eine minimale Variabilität von Tier zu Tier, die Verdoppelung des Tumorvolumens erfolgt alle 6 Tage (SC) bzw. alle 11 Tage (OT). While the tumor growth rates are different for each implant site the mice typically reach evaluation size (~750mm3 or 1E+09 p/s) in approximately 30 days post implant (See Figures 5 [SC], 6, 7, and 8 [OT]).
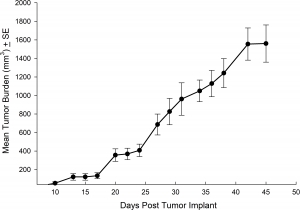
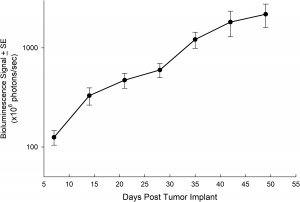
Abb. 5: Mittlere subkutane NCI-1703-Tumorlast
Fig. 6: Mittlere Tumorlast nach orthotopischer Implantation von NCI-1703
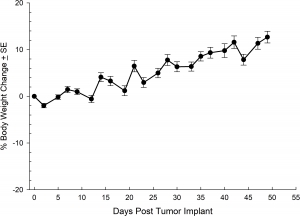
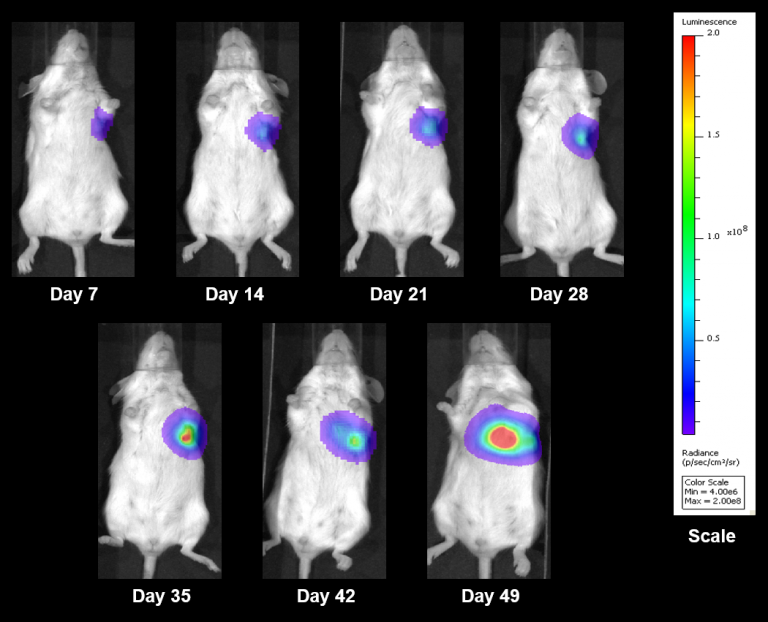
Abb. 7: Änderung des Körpergewichts in % nach orthotopischer Implantation von NCI-H1703
Abb. 8: Repräsentative BLI-Bilder nach orthotopischer Implantation von NCI-H1703
PC-9
PC-9 wurde 1989 aus einem männlichen Lungenadenokarzinom-Patienten isoliert. Es wurde gezeigt, dass PC-9 sehr empfindlich gegenüber Gefitinib und anderen EGFR-Tyrosinkinasehemmstoffen ist. Es wurde jedoch gezeigt, dass eine längere Exposition von PC-9-Zellen gegenüber EGFR-Inhibitoren zum Erwerb der T790M-Mutation und einer resistenten Zelllinie führen kann. Dieses Modell wäre wertvoll bei der Bewertung von EGFR-Inhibitoren der nächsten Generation oder möglicherweise bei der Entwicklung einer resistenten Version zur Bewertung alternativer Behandlungsansätze. We have developed PC-9 as a subcutaneous model that demonstrates reliable growth with minimal animal-to-animal variability. Die Verdopplungszeit des Tumorvolumens beträgt ca. 7 Tage und die Tumoren erreichen typischerweise eine Bewertungsgröße (ca. 750 mm3) ungefähr 28 Tage nach der Implantation (siehe Abbildungen 9).
Please contact us if you are interested in discussing any of our human NSCLC models.
Investigate our full list of human xenograft models, including our extensive NSCLC Bank.
Abb. 9: Mittlere subkutane PC-9-Tumorbelastung
Verweise
2EML4-ALK fusion gene and efficacy of an ALK kinase inhibitor in lung cancer. Jussi P. Koivunen, Craig Mermel, Kreshnik Zejnullahu, Carly Murphy, Eugene Lifshits,6 Alison J. Holmes, Hwan Geun Choi, Jhingook Kim, Derek Chiang, Roman Thomas, Jinseon Lee,9,10 William G. Richards, David J. Sugarbaker, Christopher Ducko, Neal Lindeman, J. Paul Marcoux, Jeffrey A. Engelman, Nathanael S. Gray, Charles Lee, Matthew Meyerson und Pasi A. Jänne. Clin Cancer Res. 2008 Jul 1; 14(13): 4275–4283.
3Stromal Platelet-Derived Growth Factor Receptor α (PDGFRα) Provides a Therapeutic Target Independent of Tumor Cell PDGFRα Expression in Lung Cancer Xenografts. David E. Gerber, Puja Gupta, Michael T. Dellinger, Jason E. Toombs, Michael Peyton, Inga Duignan, Jennifer Malaby, Timothy Bailey, Colleen Burns, Rolf A. Brekken und Nick Loizos Molecular Cancer Therapeutics 10,12/1535–7163.MCT-12–0431. Herausgegeben im November 2012.
Unterhalten wir uns
Kontakt