Author: Sheri Barnes, PhD, Director, Scientific Development
Datum: October 2017
Forscher verwenden präklinische Mausmodellierung, um konventionelle Behandlungsmethoden für Lymphome wie Strahlen- und Chemotherapie in Kombination mit immunmodulierenden Wirkstoffen einzusetzen, um diese Krankheit wirksamer zu behandeln. We have developed the syngeneic A20 tumor model, a B cell lymphoma, to support these immuno-oncology applications.
Lymphome stellen einen sehr heterogenen Satz von malignen lymphoiden Zellen dar. Sie können entweder von B- oder T-Zellen stammen, aber von B-Zellen abgeleitete Lymphome, insbesondere Non-Hodgkin-Lymphome (NHL), sind am häufigsten. Lymphome können bei Kindern und Jugendlichen diagnostiziert werden, aber die Inzidenz von Lymphomen steigt mit dem Alter signifikant an, wobei das mittlere Diagnosealter 67 Jahre beträgt. 2017 werden schätzungsweise 72,24 neue Fälle von NHL in den Vereinigten Staaten diagnostiziert werden und 20,14 Patienten werden daran sterben. Während die 5-Jahres-Überlebensrate für NHL mit 71 % relativ hoch ist, ist ein erneutes Auftreten innerhalb von fünf Jahren nach der Behandlung am häufigsten, 1 was die Entwicklung neuer Behandlungsstrategien für Lymphome für ein langfristiges Überleben dieser Patienten unerlässlich macht.
Aufgrund des Einflusses der Immuntherapie auf andere Krebsarten nutzen Forscher präklinische Mausmodellierung, um konventionelle Behandlungsmethoden für Lymphome wie Strahlen- und Chemotherapie in Kombination mit immunmodulierenden Wirkstoffen einzusetzen, um diese Krankheit wirksamer zu behandeln. We have developed the syngeneic A20 tumor model, a B cell lymphoma, to support these immuno-oncology applications. A20 wurde von einem spontan auftretenden Retikulumzell-Sarkom einer alternden Balb/c-Maus abgeleitet. 2 A20-Tumoren zeigen nachweislich hohe PD-L{[ #3]}-Spiegel auf und sprechen auf immunmodulatorische Antikörper an. Zusammengenommen ist A20 ein attraktives Modell für die Entwicklung von Wirkstoffen für die Immuntherapie.
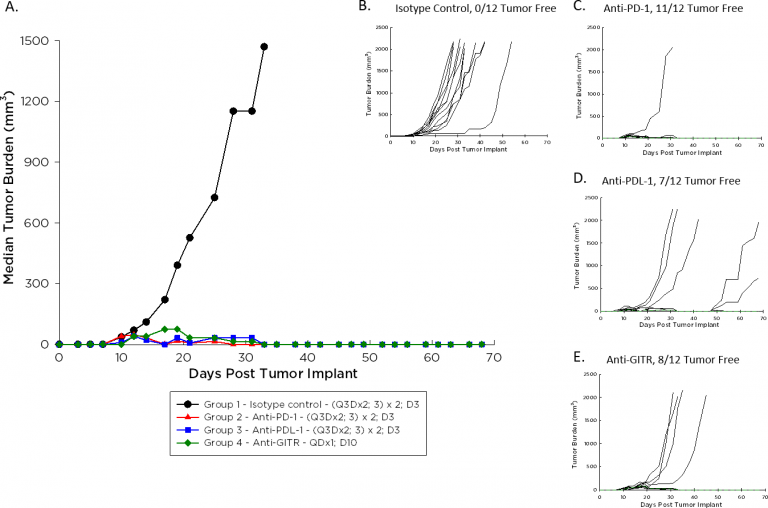
Die Verdopplungszeit von A20 beträgt ca. 4 bis 5 Tage, eine moderate Wachstumsrate im Vergleich zu anderen syngenen Modellen, was möglicherweise eine längere Dosierungsdauer für Testmittel bedeutet, um deren Antitumoraktivität auszulösen. Abbildung 1 zeigt das mittlere (1A) und individuelle (B–E) Wachstum von Kontrolltumoren im Vergleich zu denen, die mit einem immunmodulatorischen Antikörper behandelt wurden. Mit Dosierung am Tag 3 nach der Implantation für die Checkpoint-Hemmstoffe Anti-PD-1 und Anti-PD-L1 und am Tag 10 nach der Implantation für den Agonisten Anti-GITR ist die Antitumorreaktion auffällig. Wir erwarten, dass die Einleitung der Dosierung mit diesen Wirkstoffen, sobald A20-Tumore tastbar sind, in Kombination mit Kandidatenmolekülen Raum für Verbesserungen bietet.
Abb. 1: Mittleres und individuelles Wachstum von A20-Tumoren nach Immuntherapie
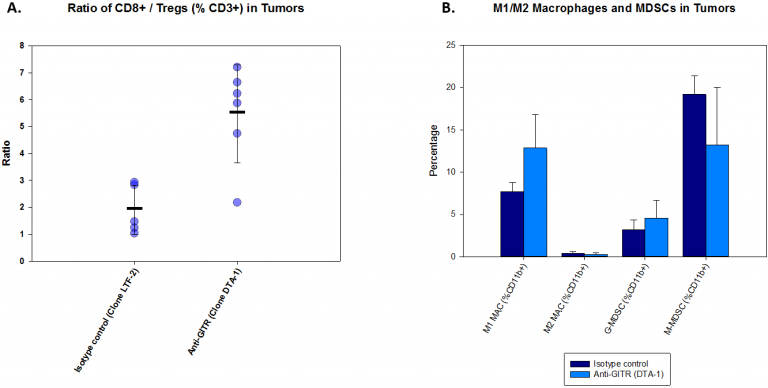
Um die immunmodulatorischen Wirkungen von Anti-GITR auf den A20-Tumor zu untersuchen, analysierten wir eine Woche nach der Behandlung T-Zell- und myeloide Zellpopulationen im Tumor. Die Ergebnisse sind in Abbildung 2 dargestellt. Bei einer Anti-GITR-Behandlung steigt das CD8+/Treg-Verhältnis dramatisch an (Abb. 2A). Dieser Anstieg weist auf eine Beteiligung des Immunsystems des Wirts hin, die sich auch in einer Abnahme der Tumorlast widerspiegelt (Abb. 1). Im Gegensatz dazu waren die Veränderungen der myeloischen Zellpopulationen gering. Während einige myeloide Zellpopulationen während der Behandlung unverändert blieben, sind bei einer Anti-GITR-Behandlung im Vergleich zur Isotypkontrolle Tendenzen zu einer Abnahme von %M-MDSC bei gleichzeitiger Zunahme von %M 1-Makrophagen erkennbar (Abb. 2B).
Abb. 2: Immunprofilierung von A20-Tumoren nach Anti-GITR-Behandlung
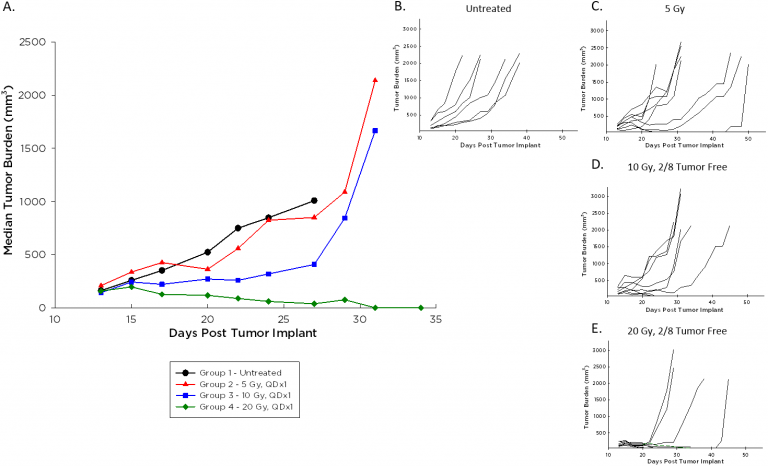
Neben der Zusage einer Immuntherapie wird die Strahlentherapie häufig im Verlauf der klinischen Lymphombehandlung eingesetzt und typischerweise in Kombination mit anderen Wirkstoffen verabreicht. We employ the Small Animal Radiation Research Platform (SARRP) by XStrahl for modeling focal beam radiation (see our related blog and poster), and investigated a single dose range of 5-20 Gy against A20 tumors. Das mittlere (Abbildung 3A) und individuelle (Abbildung 3B–E) Tumorwachstum nach dieser Behandlung ist unten dargestellt. A20-Tumore sind von Strahlung in allen Dosen betroffen, und zwei Mäuse mit den Dosierungen 10 und 20 Gy zeigten dauerhafte vollständige Reaktionen fast 70 Tage nach der Implantation. Diese Tiere blieben trotz einer erneuten Herausforderung mit einer zweiten Injektion von A20-Zellen tumorfrei, während Tumore bei naiven Tieren desselben Alters wie erwartet wuchsen (Daten nicht gezeigt).
Abb. 3: Mittlere und individuelle Wachstumskurven von A20-Tumoren nach fokaler Bestrahlung
Das A20-Modell bietet robuste präklinische Mittel zur Untersuchung von B-Zell-Lymphomen. Die Reaktion von A20 auf Checkpoint-Hemmstoffe, kostimulatorische Immunoagonisten und Strahlentherapie macht es zu einem attraktiven Modell für den Einsatz in der präklinischen Immunonkologie.
Verweise
1Howlader N, Noone AM, Krapcho M, Miller D, Bishop K, Kosary CL, Yu M, Ruhl J, Tatalovich Z, Mariotto A, Lewis DR, Chen HS, Feuer EJ, Cronin KA (eds). SEER Cancer Statistics Review, 1975–2014, National Cancer Institute. Bethesda, MD, https://seer.cancer.gov/csr/1975_2014/, basierend auf der SEER-Datenübermittlung von November 2016, veröffentlicht auf der SEER-Website, April 2017.
2Kim KJ, Kanellopoulos Langevin C, Merwin RM, Sachs DH, Asofsky R (1979) Establishment and characterization of BALB/c lymphoma lines with B cell properties. Journal ofImmunology, 122(2): 549–554.
Unterhalten wir uns
Kontakt